
腫瘤相關成纖維細胞(Cancer-associated fibroblasts,CAFs)是腫瘤微環境中最關鍵的成分之一,其在腫瘤發生、發展過程中起著至關重要的作用,并被認為是具有重大價值的癌癥治療靶標。然而,CAFs的表型和功能異質性阻礙了腫瘤的研究與治療的應用。盡管人們越來越認識到CAFs的多樣性,CAFs上用于精確治療的表面標記物仍然十分有限。在2018年發表在Cell雜志上的文章中,我校孫逸仙紀念醫院宋爾衛院士、蘇士成教授團隊通過對比耐藥和敏感乳腺癌標本中成纖維細胞的表達譜,利用CD10、GPR77這兩個差異表達的膜蛋白,成功鑒定出一個新的CD10+GPR77+成纖維細胞亞群,并發現其對乳腺腫瘤干性的維持和化療耐受起著關鍵作用。
機制上,CD10+GPR77+CAFs通過p65磷酸化和乙酰化作用持續地被NF-κB激活而被驅動,而這種作用是通過GPR77(一種C5a受體)的補體信號傳導來維持的。但CD10在這個過程中所起的作用和機制仍未完全闡明。近日,我校孫逸仙紀念醫院蘇士成教授團隊揭示了腫瘤相關成纖維細胞上的CD10維持乳腺癌干性的新機制,研究成果于2021年8月7日在國際著名期刊Advanced Science發表,題為“A CD10-OGP Membrane Peptolytic Signaling Axis in Fibroblasts Regulates Lipid Metabolism of Cancer Stem Cells via SCD1”。
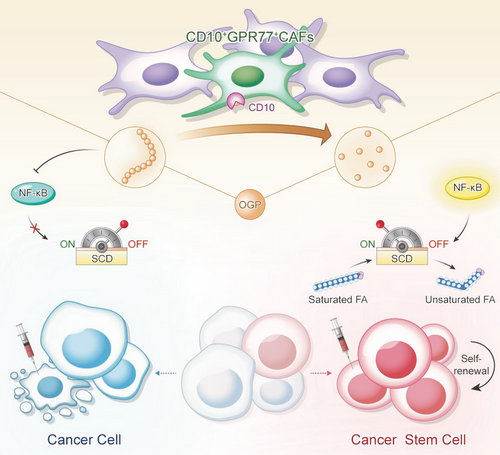
研究發現圖示
孫逸仙紀念醫院蘇士成教授是本論文的唯一通訊作者,余樹斌、陸藝文、蘇安博士為該論文的共同第一作者。該研究發現了腫瘤相關成纖維細胞上的肽鏈內切酶CD10能夠水解并失活腫瘤微環境中的成骨生長肽(Osteogenic growth peptide, OGP),從而維持乳腺腫瘤細胞干性和促進腫瘤化療耐受。機制上,OGP通過激活GPCR受體抑制了NFκB信號通路活性,從而抑制受其調控的SCD1表達。SCD1是合成單不飽和脂肪酸過程中的限速酶,該酶能夠影響腫瘤的脂不飽和度,進而維持腫瘤細胞的干性。總的來說,CAF上的CD10通過一個肽水解信號影響了腫瘤干細胞的脂代謝,進而維持了腫瘤細胞的干性和促進腫瘤化療耐受。
蘇士成教授團隊的研究成果揭示了腫瘤微環境維持腫瘤細胞干性的新機制,發現并證實了靶向腫瘤相關成纖維細胞上的CD10能夠改善乳腺癌的化療療效,為乳腺癌的治療和診斷提供了新的靶點。
論文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202101848