
中大新聞網(wǎng)訊(通訊員王文濤)N6-甲基腺嘌呤(N6-methyladenosine, m6A) 是真核生物mRNA或長(zhǎng)鏈非編碼RNA的最普遍的修飾之一,RNA m6A修飾的失調(diào)與癌癥的發(fā)生發(fā)展密切聯(lián)系。然而,關(guān)于維持細(xì)胞RNA m6A修飾內(nèi)穩(wěn)態(tài)的分子機(jī)制仍不清楚。
中山大學(xué)生命科學(xué)學(xué)院王文濤副教授團(tuán)隊(duì)發(fā)現(xiàn),在細(xì)胞中,METTL14遠(yuǎn)比METTL3蛋白水平低,而且METTL14不能單獨(dú)穩(wěn)定存在,是RNA m6A內(nèi)穩(wěn)態(tài)的決定因素。有趣的是,METTL14在多種細(xì)胞內(nèi)難以單獨(dú)過(guò)表達(dá),必須同時(shí)回補(bǔ)METTL3才能實(shí)現(xiàn)高效表達(dá),提示細(xì)胞內(nèi)METTL3在維持METTL14蛋白穩(wěn)定方面起著重要作用。進(jìn)一步驗(yàn)證發(fā)現(xiàn)METTL3 450-454aa和464-480aa氨基酸結(jié)構(gòu)域,而非催化位點(diǎn)序列對(duì)保護(hù)METTL14穩(wěn)定性至關(guān)重要。隨后,該團(tuán)隊(duì)率先鑒定了METTL14三個(gè)主要的賴(lài)氨酸泛素化修飾位點(diǎn),分別是K148、K156、K162,以及揭示了STUB1作為E3泛素連接酶精確調(diào)控METTL14泛素化降解的分子機(jī)制。該成果成功解釋了m6A調(diào)控復(fù)合體中,METTL3對(duì)METTL14的保護(hù)作用,并發(fā)現(xiàn)細(xì)胞中METTL3-METTL14-STUB1調(diào)控模式對(duì)維持細(xì)胞內(nèi)m6A動(dòng)態(tài)平衡的重要作用。
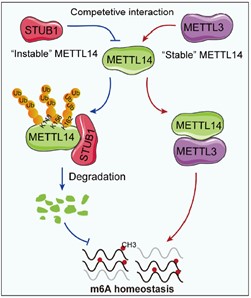
METTL14蛋白代謝及RNA m6A細(xì)胞內(nèi)穩(wěn)態(tài)
綜上,該工作率先發(fā)現(xiàn)METTL14是調(diào)控RNA m6A修飾平衡的關(guān)鍵因素,揭示了METTL3競(jìng)爭(zhēng)結(jié)合METTL14逃逸E3連接酶STUB1介導(dǎo)其泛素化降解,維持細(xì)胞內(nèi)m6A動(dòng)態(tài)平衡的分子機(jī)制。這也是首次揭示了METTL3/STUB1的結(jié)合競(jìng)爭(zhēng)模型在維持METTL14代謝和m6A修飾平衡中的重要作用,提示通過(guò)提高STUB1表達(dá)精確調(diào)控METTL14泛素化降解以及m6A水平可能是潛在治療惡性癌癥的一種有效策略。
該研究以“METTL3 protects METTL14 from STUB1-mediated degradation to maintain m6A homeostasis”為題的研究論文發(fā)表在EMBO reports。生命科學(xué)學(xué)院王文濤副教授,為該項(xiàng)工作的唯一通訊作者,生命科學(xué)學(xué)院博士畢業(yè)生曾展城和博士研究生潘琦為本文共同第一作者。生命科學(xué)學(xué)院陳月琴教授為論文進(jìn)行了重要指導(dǎo)和大力支持。孫逸仙紀(jì)念醫(yī)院何波和葉華教授對(duì)研究提供了重要支持。相關(guān)工作得到了國(guó)家重點(diǎn)研發(fā)計(jì)劃(No.2021YFA1300502)、國(guó)家自然基金(No.32170570 和 81772621),廣東省杰出青年基金(No. 2021B1515020002)和廣州市科技計(jì)劃項(xiàng)目支持(No.202102020070)。
論文鏈接:https://www.embopress.org/doi/epdf/10.15252/embr.202255762#accessDenialLayout