
中大新聞網訊(通訊員陳永明)人體內過量的游離核酸可被核酸感受器識別而引起先天性免疫反應,釋放出腫瘤壞死因子TNF-a或I型干擾素而產生嚴重的自身免疫疾病。陽離子聚合物可清除游離核酸而抑制其引起的炎癥反應(團隊前期研究:Nat Commun 2018; Angew Chem 2019; Sci Adv 2020; Adv Funct Mater 2020; Biomaterials 2021, 2022),然而陽離子聚合物材料存在較大的細胞毒性,在應用中可能存在安全風險,并且被材料結合游離核酸的藥代也需要闡明。為了解決這一問題,中山大學材料科學與工程學院陳永明和劉利新團隊采用寡聚乙二醇化的聚咪唑模擬天然DNA酶來催化磷酸二酯鍵的水解,從而緩解與游離核酸相關的自身免疫疾病如類風濕性關節炎、Aicardi-Goutières綜合征的癥狀。
許多天然的核酸水解酶以咪唑基團作為功能基團來催化磷酸二酯鍵的斷裂,因此該項研究用側掛咪唑基團的合成聚合物,并用寡聚乙二醇側基以提高材料的水溶性和生物相容性,延長體內的滯留時間。由于該人工核酸酶采用的咪唑基團是比脂肪胺更弱的有機堿,對細胞和組織具有更好的生物安全性,解決了陽離子材料在體內使用的安全隱患。模擬酶在體內可降解游離核酸,有效抑制了相關炎癥反應(圖1)。
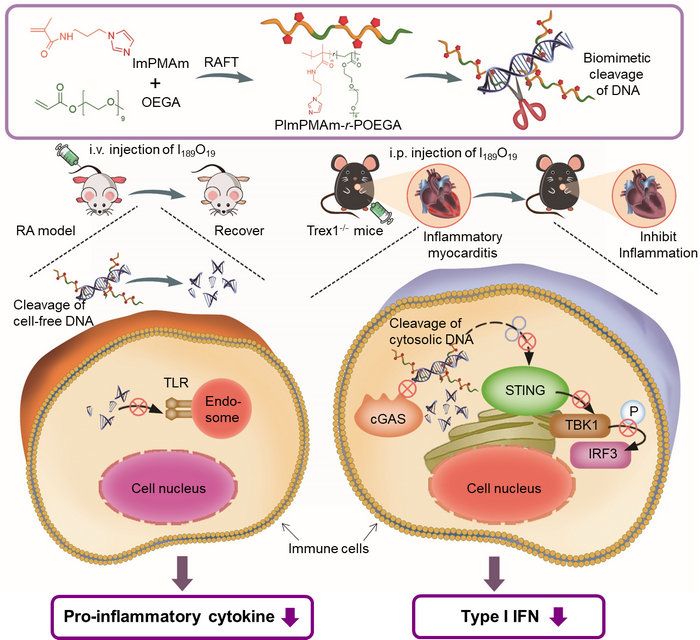
圖1 聚咪唑通過模擬DNA水解酶的水解來抑制自身免疫疾病中DNA引起炎癥的示意圖,本報道在類風濕性關節炎和Aicardi-Goutières綜合征動物模型上進行了驗證。
通過可控聚合反應,作者合成了四種不同咪唑和寡聚乙二醇的聚合物:I195、I189O19、I225O74和I238O132。提高寡聚乙二醇的含量雖然能提高材料水溶性,但是也會降低了咪唑基團的密度而降低了催化磷酸二酯鍵斷裂的效率。適量寡聚乙二醇的聚咪唑I189O19可保持一定高的咪唑基團密度,具有有效的DNA水解效率,也表現出良好的生物相容性,從而能安全和有效地抑制由核酸引起的細胞內Toll樣受體的激活(圖2A-C)。
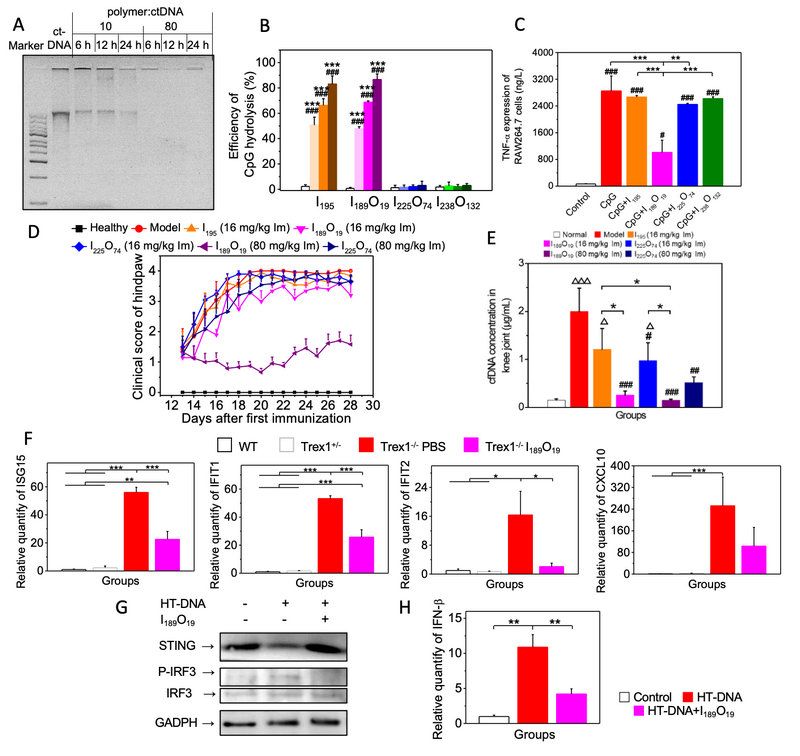
圖2 (A、B)不同組成聚合物模擬酶催化DNA的水解能力表征;(C)模擬酶抑制RAW264.7細胞分泌細胞因子;(D)模擬酶對CIA大鼠模型后爪腫脹得分的影響;(E)聚咪唑材料治療后CIA大鼠關節游離核酸的含量變化;(F)聚咪唑I189O19抑制Trex1缺陷小鼠中由細胞質DNA誘導的炎癥,不同組的小鼠心臟中干擾素刺激基因的mRNA水平;聚咪唑I189O19抑制RAW264.7細胞內HT-DNA引起的(E)STING降解和IRF3的磷酸化,以及(F)IFN-b的表達。
該類聚咪唑可以抑制類風濕性關節炎CIA大鼠的炎癥反應(圖2D)。寡聚乙二醇的引入可以使得聚咪唑的水溶性增加而提高可注射的劑量,靜脈注射高劑量的I189O19可獲得比其他治療組更有效的治療效果,包括更好地抑制關節的腫脹、減少軟骨的侵蝕、減少炎癥細胞在滑膜的浸潤等。同時,寡聚乙二醇能夠提高材料在體內循環時間,降低材料在體內代謝的速率,從而提高在炎癥關節處的滯留時間,更好地降解關節處多余的游離核酸(圖2E),降低關節滑膜處IL-6和TNF-α等炎癥因子水平以及MMP-3水平。
作者進一步研究聚合物模擬酶在Trex1酶缺失的小鼠的治療效果。天然的Trex1酶缺陷導致機體細胞質DNA聚集, 使得cGAS介導I型干擾素的激增,從而引發遺傳性Aicardi-Goutiéres綜合征。動物實驗證明七天腹腔注射I189O19可以有效地下調Trex1敲除小鼠心臟中干擾素刺激基因的水平(圖2F),減少炎癥細胞的浸潤。研究還發現I189O19可有效地降解細胞質DNA,阻斷由細胞質DNA如HT-DNA引起的STING的降解和IRF3的磷酸化,抑制IFN-b的表達(圖2G,H)。
該工作揭示了聚合物基模擬DNA酶可有效降解體內多余的DNA并抑制相關免疫炎癥反應,可通過降解炎癥關節處的游離核酸來有效地抑制類風濕性關節炎的癥狀,可以在DNA酶缺失的小鼠模型中彌補DNA酶來抑制由多余DNA引起的炎癥反應。因此,這種模擬DNA酶不僅可以降低自身免疫疾病中由于游離核酸引起的免疫反應,更能替補體內缺失的DNA酶抑制如Aicardi-Goutières綜合征中由細胞內DNA引起的炎癥反應。綜上所述,該工作為治療自身免疫疾病和自身炎癥疾病提供了一種簡單、安全、有效的新策略。
相關研究結果以“A Tailored Artificial DNase Blocks Sensor Activation and Prevents Autoimmune and Autoinflammatory Diseases”為題,于2023年2月28日發表在材料領域期刊Advanced Functional Materials。材料科學與工程學院博士研究生梁慧怡和杜逸博為該論文的共同第一作者,劉利新教授、陳永明教授為論文的共同通訊作者。中山大學材料科學與工程學院為論文第一完成單位。該研究工作得到國家自然科學基金資助。