
中大新聞網(wǎng)訊(通訊員胡友金、唐艷麗)視網(wǎng)膜神經(jīng)發(fā)育和再生的分子機(jī)制復(fù)雜,涉及DNA變異、表觀遺傳修飾、RNA轉(zhuǎn)錄和剪接等,多組學(xué)整合分析被認(rèn)為是揭示神經(jīng)干細(xì)胞譜系分化和再生分子機(jī)制的有效手段。由于神經(jīng)發(fā)育和再生過程中多個(gè)神經(jīng)譜系交錯(cuò)在一起,如何準(zhǔn)確地分辨不同譜系并系統(tǒng)描繪其多維分子特征的動(dòng)態(tài)變化,是精準(zhǔn)解析其分子機(jī)制的關(guān)鍵所在。近年來,單細(xì)胞多組學(xué)測(cè)序技術(shù)的發(fā)展,為分析神經(jīng)元發(fā)育和再生復(fù)雜分子機(jī)制提供了有力方法。然而,RNA可變剪接作為調(diào)控基因功能的重要環(huán)節(jié),尚缺乏有效的單細(xì)胞多組學(xué)關(guān)聯(lián)分析方法。
2024年9月13日,中山大學(xué)中山眼科中心胡友金教授團(tuán)隊(duì)在Nature Communications雜志在線發(fā)表了題為“Simultaneous profiling of RNA isoforms and chromatin accessibility of single cells of human retinal organoids”的研究論文,報(bào)道了一種名為scRICA-seq (single-cell RNA isoform and chromatin accessibility sequencing) 的單細(xì)胞多組學(xué)測(cè)序方法,該技術(shù)能夠同時(shí)檢測(cè)單細(xì)胞水平染色質(zhì)可及性、RNA表達(dá),以及 isoform全長(zhǎng)結(jié)構(gòu),實(shí)現(xiàn)了單個(gè)細(xì)胞水平的表觀遺傳學(xué)、轉(zhuǎn)錄與RNA剪接的整合分析,為揭示視網(wǎng)膜神經(jīng)元發(fā)育和再生的新機(jī)制提供技術(shù)支撐。
胡友金團(tuán)隊(duì)長(zhǎng)期專注于單細(xì)胞測(cè)序技術(shù)的創(chuàng)新開發(fā)。早在2020年,該團(tuán)隊(duì)已在《Nature Communications》上發(fā)表scRCAT-seq技術(shù),用于RNA isoform的檢測(cè)。此次,團(tuán)隊(duì)進(jìn)一步改進(jìn)原有方法,發(fā)展了scRCAT-seq2全長(zhǎng)轉(zhuǎn)錄組測(cè)序技術(shù),并結(jié)合10x Genomics的Chromium Next GEM Single Cell Multiome ATAC + Gene Expression平臺(tái),實(shí)現(xiàn)了染色質(zhì)可及性與RNA isoform同時(shí)檢測(cè)的多組學(xué)方法。其中,scRCAT-seq2的核心技術(shù)是通過單分子成環(huán)技術(shù)處理cDNA,并將覆蓋TSS,TES和exon的測(cè)序序列進(jìn)行同一標(biāo)簽標(biāo)記,并組裝構(gòu)建全長(zhǎng)cDNA序列。(圖1)
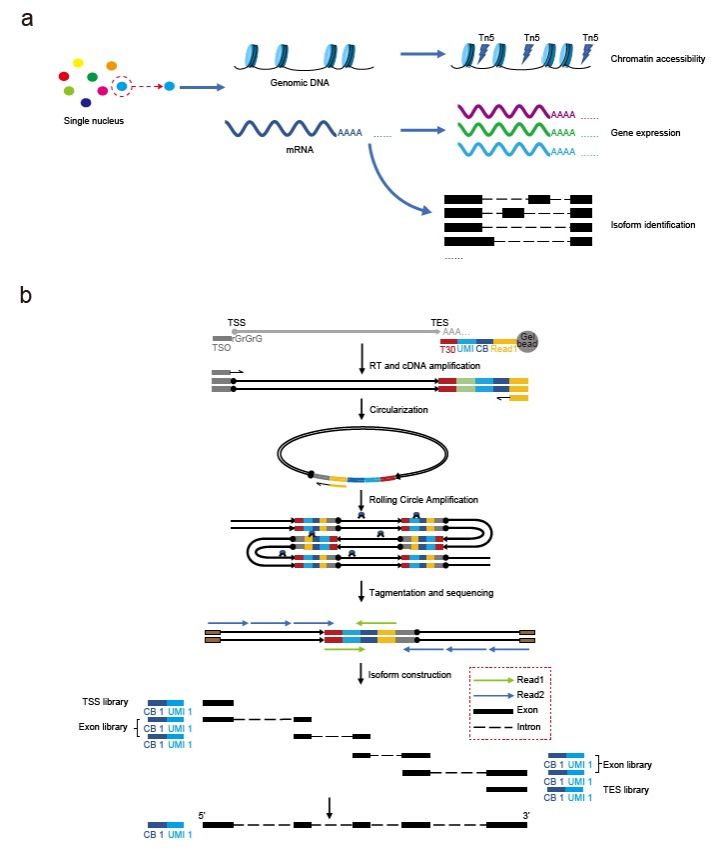
圖1:scRICA-seq和scRCAT-seq2的示意圖
研究者將scRCAT-seq2在低通量與高通量條件下與多種三代測(cè)序技術(shù)(如SCAN-seq2、scISOr-seq、HIT-scISO-seq等)進(jìn)行對(duì)比分析,結(jié)果顯示scRCAT-seq2在成本效益和檢測(cè)靈敏度方面均具有顯著優(yōu)勢(shì)。(圖2)
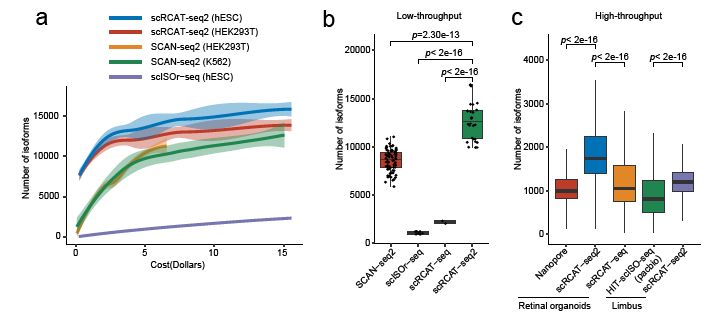
圖2:scRCAT-seq2與其他方法比較分析圖
研究者將scRICA-seq應(yīng)用于人類視網(wǎng)膜發(fā)育過程,構(gòu)建了人類視網(wǎng)膜類器官的單細(xì)胞多組學(xué)圖譜。基于單細(xì)胞異構(gòu)體的聚類分析,確定了六個(gè)細(xì)胞簇,對(duì)應(yīng)于六種典型的視網(wǎng)膜早期神經(jīng)元,包括視網(wǎng)膜祖細(xì)胞(RPCs)、視網(wǎng)膜神經(jīng)節(jié)細(xì)胞(RGCs)、無(wú)長(zhǎng)突細(xì)胞/水平細(xì)胞(AC/HCs)、視錐細(xì)胞前體(PR precursors)、神經(jīng)生成RPCs(neurogenic RPCs)以及視錐細(xì)胞(cones),其結(jié)果與scRNA-seq技術(shù)所得數(shù)據(jù)高度一致。(圖3)

圖3:基于scRICA-seq的人類視網(wǎng)膜類器官的多組學(xué)單細(xì)胞圖譜
進(jìn)一步,作者研究了RPC分化為cone過程中RNA isoform的動(dòng)態(tài)選擇模式,發(fā)現(xiàn)cone和RPC之間共有2292種差異表達(dá)的isoform,其中1143種isoform在cone中高度表達(dá),1149種在RPC中高度表達(dá)。通過轉(zhuǎn)錄因子motif分析,研究者預(yù)測(cè)了589個(gè)可能與這些動(dòng)態(tài)調(diào)節(jié)的剪接位點(diǎn)結(jié)合的轉(zhuǎn)錄因子。在預(yù)測(cè)的轉(zhuǎn)錄因子中包含了11種先前報(bào)道的參與調(diào)節(jié)RNA剪接的轉(zhuǎn)錄因子,包括NEUROD1、SP1和KLF4等,同時(shí)還包含了已知的細(xì)胞命運(yùn)決定因子,如NEUROD1、ASCL1和THRB等。這提示,剪接位點(diǎn)染色質(zhì)可及性的動(dòng)態(tài)變化與RNA剪接可能協(xié)同調(diào)控細(xì)胞命運(yùn)決定(圖4)。
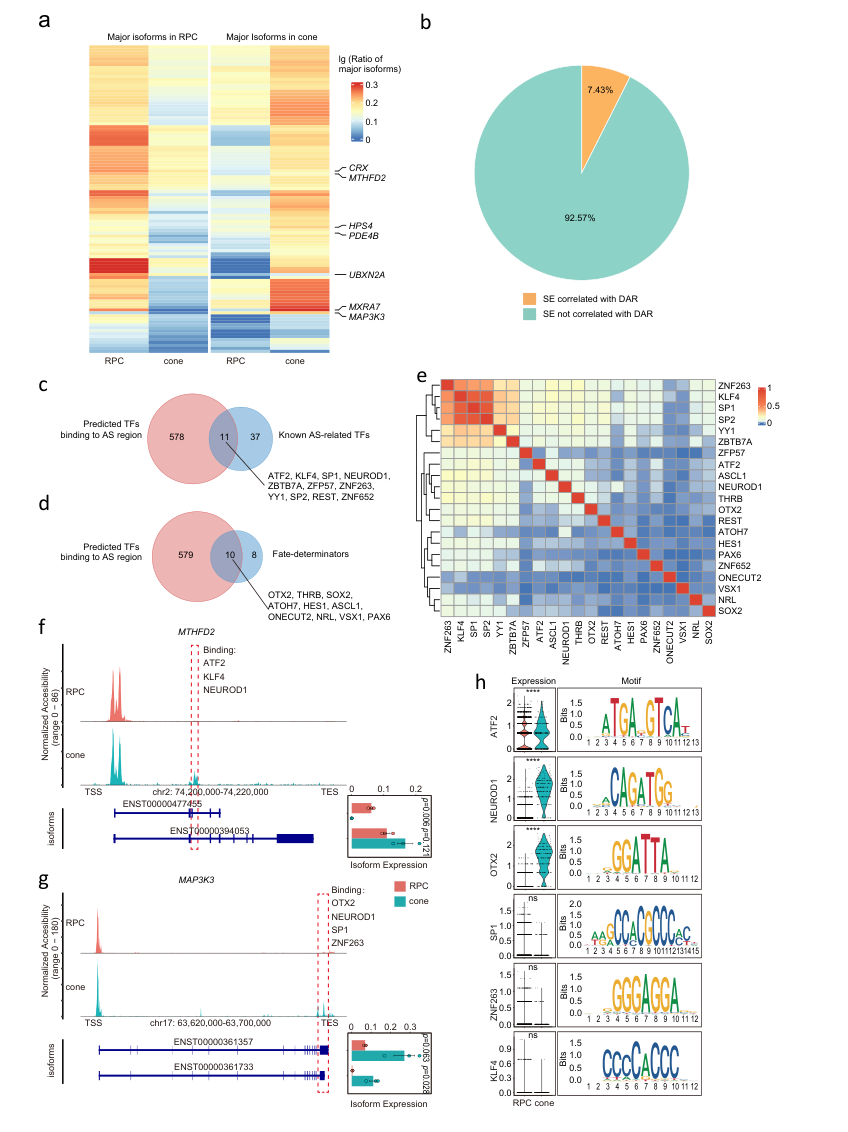
圖4:RPC發(fā)育過程中RNA isoform選擇與染色質(zhì)可及性和TFs的相關(guān)性
綜上所述,scRICA-seq在單細(xì)胞水平實(shí)現(xiàn)了表觀遺傳學(xué)、RNA轉(zhuǎn)錄和剪接的整合分析,發(fā)現(xiàn)染色質(zhì)可及性和命運(yùn)決定因子協(xié)同調(diào)控下游基因的表達(dá)和轉(zhuǎn)錄剪接,為闡明視網(wǎng)膜神經(jīng)元發(fā)育和命運(yùn)決定的機(jī)制提供了新思路。
本研究由中山大學(xué)中山眼科中心胡友金教授課題組完成。中山眼科中心張淑堯(研究助理)、肖玉華(博士研究生)、莫新枝(研究助理)為共同第一作者,胡友金教授為唯一通訊作者。中山大學(xué)中山眼科中心、眼病防治全國(guó)重點(diǎn)實(shí)驗(yàn)室為第一作者單位和通訊作者單位。
論文鏈接:
https://www.nature.com/articles/s41467-024-52335-0