
近日,我校附屬口腔醫院王焱、程斌教授團隊在國際知名期刊Bioactive Materials (中科院一區,IF=8.724)發表題為“Bioadaptation of implants to in-vitro and in-vivo oxidative stress pathological conditions via nanotopography-induced FoxO1 signaling pathways to enhance osteoimmunal regeneration”的論文,發現納米形貌鈦表面在氧化應激狀態下可通過直接和間接的骨免疫調節作用在一定程度上減輕病理狀態對骨再生過程的影響,同時進一步揭示叉頭框蛋白轉錄因子1(FoxO1)介導的抗氧化功能是納米形貌鈦表面促進氧化應激狀態下免疫骨再生的重要機制,有望為鈦種植體表面改性提供新思路。
該研究由我校附屬口腔醫院王焱、程斌教授團隊以及我校附屬第一醫院口腔頜面外科王安訓教授合作完成,博士生黃靜燕和碩士生李若琪為共同第一作者。研究工作依托于附屬口腔醫院廣東省口腔醫學重點實驗室完成,并得到廣東省高水平醫院建設專項資金資助。
隨著人口老齡化社會的到來,衰老及代謝相關性疾病包括骨質疏松、糖尿病等疾病的發病率逐漸升高,而這些疾病也嚴重影響口腔種植治療的效果,成為口腔種植的相對禁忌癥。研究病理狀態下種植界面成骨過程的改變、通過植入材料的表面改性達到提高成骨作用是該領域亟待解決的問題。近十多年來研究顯示氧化應激是這類衰老及衰老相關性疾病的重要發病機制,但關于氧化應激狀態對鈦種植體材料成骨能力的影響及相關機制研究卻少有報道。
王焱、程斌教授團隊采用過氧化氫、脂多糖和高糖分別模擬體內固有的、炎癥和糖尿病引發的氧化應激狀態,發現在以上各種氧化應激模型中,相比目前臨床常用的噴砂酸蝕形成的微米形貌鈦種植體表面,納米管(TNT)形貌可使粘附于其表面的骨間充質干細胞(MSC)具備更佳的抗氧化和成骨分化性能。進一步研究發現FoxO1因子介導了該抗氧化性能:TNT表面一方面通過更佳的親水性促進MSC粘附,并進一步促使MSC胞內FoxO1表達,從而降低胞內活性氧水平、細胞凋亡比例,并促進成骨蛋白的表達;另一方面,TNT形貌可促使巨噬細胞(Mφ)在氧化應激狀態下更多地向抑炎型極化,分泌更多的抑炎因子,影響局部免疫微環境,從而促進免疫成骨(圖1)。
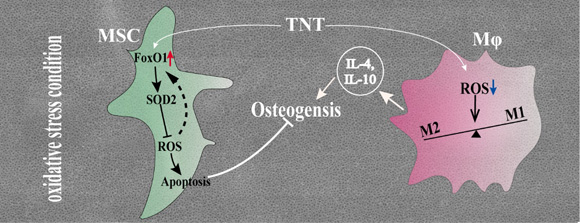
圖1 FoxO1介導納米形貌種植體促進氧化應激狀態下免疫骨再生的機制圖
在糖尿病大鼠這一氧化應激動物模型中,納米管形貌種植體周圍骨組織也表現出一定的抗氧化和抗炎作用,且種植體-骨接觸率較噴砂酸蝕種植體更高,骨整合效果更好,提示了TNT形貌種植體在糖尿病等病理條件的應用潛能。上述體內外研究為探索氧化應激狀態下納米形貌鈦表面的骨免疫再生機制及今后的臨床運用提供了有力的實驗室基礎。
論文鏈接:https://www.sciencedirect.com/science/article/pii/S2452199X21000839