
中大新聞網(wǎng)訊(通訊員張黎明)近日,中山大學(xué)材料科學(xué)與工程學(xué)院張黎明教授課題組與中山大學(xué)附屬第一醫(yī)院病理科王芬副教授課題組在 International Journal of Biological Macromolecules 雜志上發(fā)表題為“Co-delivery of siAEG-1 and doxorubicin to treat osteosarcoma via nanomicelles for azide?alkyne “click” conjugation of poly(L-lysine) dendrons onto zein”的研究論文 ( 2024,264,130729 [1-11];中科院版化學(xué)一區(qū)期刊 )。該研究報(bào)道了 siAEG-1 和多柔比星 (DOX) 的共同遞送通過(guò)納米膠束在玉米蛋白上的疊氮化物-炔“點(diǎn)擊”偶聯(lián)樹(shù)狀聚賴氨酸治療骨肉瘤。
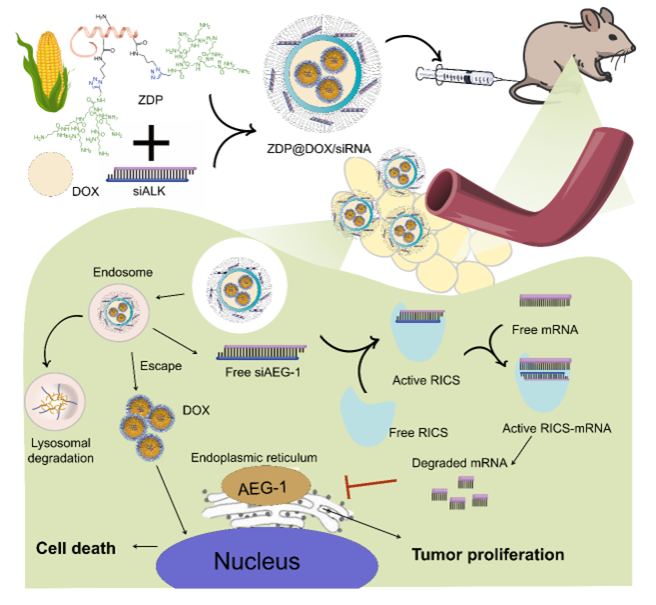
星形膠質(zhì)細(xì)胞升高基因-1 (AEG-1) 癌基因是包括骨肉瘤在內(nèi)的多種人類惡性腫瘤中一個(gè)臭名昭著且不斷發(fā)展的靶點(diǎn)。RNA干擾 (RNAi) 已被臨床證明可以有效地敲除特定基因。為了在體內(nèi)成功實(shí)施RNAi,保護(hù)載體不僅需要保護(hù)不穩(wěn)定的siRNAs不被降解,還需要將siRNAs以可控釋放的方式傳遞到靶細(xì)胞。為此,課題組合成了樹(shù)狀聚賴氨酸功能化玉米蛋白 (ZDP) 非病毒模塊化系統(tǒng),該系統(tǒng)可以在骨肉瘤中實(shí)現(xiàn)siRNA靶向的AEG-1基因沉默和抗腫瘤藥物的包封控釋。ZDP 的合理設(shè)計(jì)結(jié)合了玉米蛋白的非離子型、低免疫原性和樹(shù)狀聚賴氨酸 (DPLL) 的正電荷,通過(guò)靜電配合物包封siRNA和DOX有效載荷,在溶酶體酸性微環(huán)境中實(shí)現(xiàn)pH控制釋放。納米復(fù)合物的定向遞送在143B細(xì)胞中極大地提高了siRNA的穩(wěn)定性、攝取和AEG-1序列特異性敲除,其轉(zhuǎn)染效率與商用脂質(zhì)體相當(dāng),但具有更低的細(xì)胞毒性。這種以 AEG-1-focused RNAi 療法配合化療,抑制了143B細(xì)胞的增殖,誘導(dǎo)了143B細(xì)胞的凋亡,有效抑制了異種骨肉瘤小鼠模型的生長(zhǎng)。聯(lián)合治療是一種替代或組合策略,可以在骨肉瘤患者中產(chǎn)生持久的抑制反應(yīng)。
文章的第一作者是中山大學(xué)材料科學(xué)與工程學(xué)院龐家棟博士(已畢業(yè)),張黎明教授為論文通訊作者;文章的共同第一作者為中山大學(xué)附屬第一醫(yī)院病理科黃蕾蕾博士和碩士研究生練雅婷,共同通訊作者為王芬副教授;碩士研究生袁志潔對(duì)該論文亦有貢獻(xiàn)。本項(xiàng)研究工作得到廣東省基礎(chǔ)與應(yīng)用基礎(chǔ)研究基金自然科學(xué)基金面上項(xiàng)目、廣東省科技計(jì)劃項(xiàng)目和國(guó)家自然科學(xué)基金項(xiàng)目等的大力支持。