
中大新聞網(wǎng)訊(通訊員劉峰)DNA雙鏈斷裂 (DNA double-strand break, DSB) 是一種常見且高度有害的DNA損傷形式,其缺陷或失調(diào)與腫瘤、衰老以及免疫缺陷等密切相關(guān)。非同源末端連接(Non-homolouous end joining, NHEJ)和同源重組(Homologous recombination, HR)是DSB修復(fù)的兩條主要通路。對于富含重復(fù)序列的異染色質(zhì)來說,HR修復(fù)則容易造成非等位基因間的同源重組(non-allelic homologous recombination, NAHR),從而導(dǎo)致染色體的重排與畸變。因此,細(xì)胞如何調(diào)控和選擇這兩種途徑對DNA修復(fù)的精確性以及基因組穩(wěn)定性的維持至關(guān)重要。PARP抑制劑(PARPi)是臨床上治療BRCA突變?nèi)橄侔┖吐殉舶┑囊痪€靶向藥物,如果腫瘤細(xì)胞中NHEJ的某些關(guān)鍵調(diào)控因子如53BP1、RIF1等發(fā)生缺失或突變,則會導(dǎo)致HR通路重新激活,從而引起對PARPi的抗藥性。利用這個特性,可以通過全基因組水平的PARPi耐藥篩選,尋找一些能調(diào)控NHEJ/HR修復(fù)通路選擇且未知的NHEJ調(diào)控因子。
2023年6月15日,中山大學(xué)生命科學(xué)學(xué)院的松陽洲課題組與孫逸仙紀(jì)念醫(yī)院合作在Nature Cell Biology雜志長文發(fā)表了題為“Transmembrane nuclease NUMEN/ENDOD1 regulates DNA repair pathway choice at the nuclear periphery”的研究成果。該研究利用CRISPR篩選,首次報道了核膜錨定的核酸酶NUMEN/ENDOD1參與NHEJ修復(fù)通路,并通過特異性切割3’垂懸DNA(3’overhang DNA)調(diào)控NHEJ/HR通路的選擇。NUMEN的核膜定位為核周分布的LADs進(jìn)行NHEJ修復(fù)創(chuàng)造了條件,有利于基因組穩(wěn)定性的維持。另外,NUMEN的缺失也會導(dǎo)致BRCA1突變的腫瘤細(xì)胞對PARPi產(chǎn)生耐藥。NUMEN的發(fā)現(xiàn)解釋了細(xì)胞如何根據(jù)不同染色質(zhì)狀態(tài)以及核內(nèi)空間分布選擇最有利的DSB修復(fù)方式,以最大程度維持基因組的穩(wěn)定性。
研究人員首先通過全基因組的CRISPR敲除篩選,得到一系列可造成PARPi耐藥的候選基因,其中包括已知的耐藥基因如53BP1、RNF168與SLFN11等,證明了篩選結(jié)果的可靠性。其中,ENDOD1作為一個潛在的核酸酶,在篩選結(jié)果中排名靠前且在DNA損傷修復(fù)中的作用幾乎未見報道。基于本研究中發(fā)現(xiàn)ENDOD1的一些新特征,研究人員將其重新命名為NUMEN(Nuclear membrane endo/exonuclease)。
研究人員接著驗(yàn)證了NUMEN缺失也可導(dǎo)致腫瘤細(xì)胞對多種DNA損傷藥物更為敏感,發(fā)現(xiàn)NUMEN同時具有核酸內(nèi)切酶和3’→5’外切酶活性,能特異切割ssDNA以及3’overhang DNA,產(chǎn)生1-4 nt 5’overhang末端,推測NUMEN參與細(xì)胞內(nèi)NHEJ修復(fù)的過程。
進(jìn)一步,研究人員確認(rèn)NUMEN敲除可以使細(xì)胞核內(nèi)3’ overhang DNA累積增加,HR總體水平升高,NHEJ通路受到破壞;過表達(dá)NUMEN則有相反的效果,從而證實(shí)了NUMEN可以促進(jìn)NHEJ并抑制HR修復(fù),通過拮抗3’overhang形成參與調(diào)控DNA雙鏈損傷修復(fù)途徑的選擇。隨后,利用鄰近蛋白標(biāo)記技術(shù)(BioID),研究人員進(jìn)一步鑒定了NUMEN的相互作用蛋白組,確定了其核膜定位的生物學(xué)意義,發(fā)現(xiàn)NUMEN敲除導(dǎo)致LADs上的DSB修復(fù)效率顯著變慢。
最后,研究人員通過分析TCGA數(shù)據(jù)庫發(fā)現(xiàn),NUMEN低表達(dá)的乳腺癌樣本中,與基因組瘢痕(Genomic Scar)相關(guān)的幾種特征都有所升高;而且NUMEN表達(dá)水平與多種腫瘤的基因組拷貝數(shù)變異(CNV)呈顯著負(fù)相關(guān)。這提示NUMEN對基因組穩(wěn)定性的維持起著重要的作用。
綜上所述,該研究揭示了NUMEN作為一個新發(fā)現(xiàn)的核膜錨定核酸酶,可以對DSB末端和3’overhang DNA進(jìn)行切割,產(chǎn)生有利于NHEJ修復(fù)的底物,并調(diào)控NHEJ/HR通路的選擇。NUMEN的核膜定位促進(jìn)了LADs進(jìn)行NHEJ修復(fù),有助于基因組穩(wěn)定性的維持。
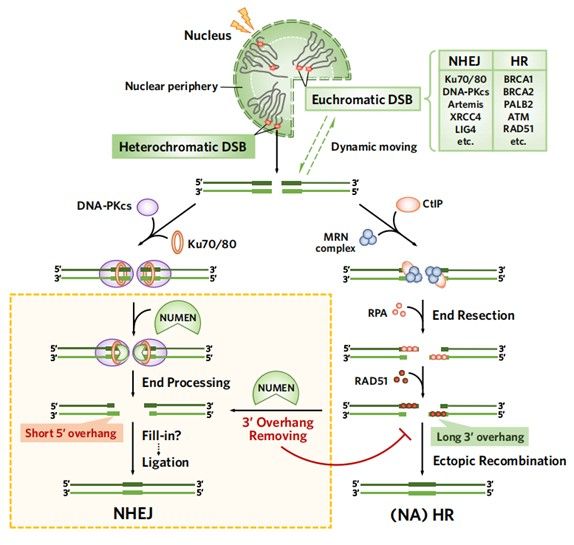
NUMEN的作用機(jī)制模型
松陽洲教授為該論文的通訊作者,陳柏洪博士以及博士研究生葛天宇為論文的共同第一作者。中山大學(xué)生命科學(xué)學(xué)院為第一署名單位。
Nature Cell Biology雜志在同期配發(fā)題為“Guiding DNA repair at the nuclear periphery”的專評,指出該工作對研究核周的DNA損傷修復(fù)通路選擇以及HRD癌癥的治療具有重要意義。