
近日,我校生命科學學院徐衛華教授團隊聯合美國俄亥俄州立大學Denlinger教授團隊在國際知名期刊PNAS上在線發表了題為“Reactive oxygen species extend insect life span using components of the insulin-signaling pathway”的研究論文,揭示了活性氧(ROS)可以通過改變胰島素信號路徑延長昆蟲生命的新機制,該研究獲得國家基金委重點項目的資助,我院博士生張小帥為該論文的第一作者,徐衛華教授和Denlinger教授為通訊作者,中山大學為第一單位。
ROS已經被定性為誘發衰老的自由基學說。近年來發現藥物處理后升高的ROS能誘導延長生命的若干例子,但是受到普遍的質疑,因為迄今為止沒有發現自然的、生理水平的ROS能延長生命的實例。
以農業害蟲棉鈴蟲的滯育(類似冬眠,和生命延長同義)為研究目標,發現了第一例自然發生的、生理水平的ROS作為胞內信號調節腦的一個獨特的胰島素信號路徑來實現生命延長 (見下圖),證明了生理水平的ROS對生物體的有益性以及延長生命的獨特機制是本項工作的核心創新點。
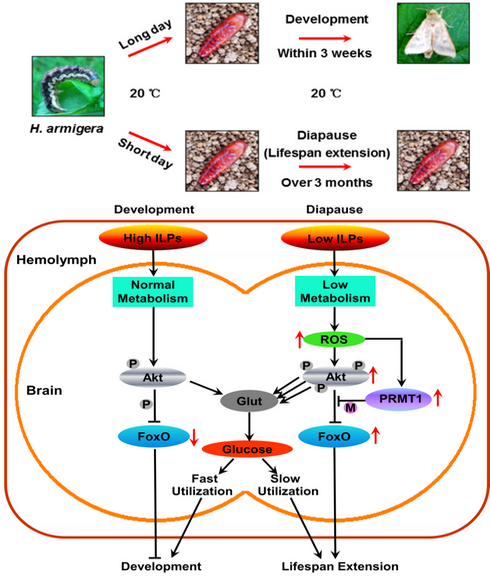
ROS通過調節胰島素信號路徑延長生命的分子機制 (ILP:胰島素類似肽)
此外,該研究工作能夠很好地解釋過去文獻報道中無法解釋的矛盾現象: 人類補充抗氧化劑(如β-胡蘿卜素、維生素A、E等)為什么增加死亡率,而不是延長生命?為什么人類運動鍛煉后補充抗氧化劑會抵消鍛煉的效果?上皮線粒體氧化損傷為什么能延遲年輕小鼠的衰老,但是卻加速年老小鼠的衰老?如果用本項研究結果就可以完美地解釋了:ROS對生物個體的有害性體現在老年期,在中青年期是有益的,這也是本項工作的創新點之一。
論文發表后,美國科學家Palli教授在PNAS上以“New roles for old actors, ROS and PRMT1”為題發表評述,全面介紹本項研究的成果,充分肯定ROS延長生命的新功能及其生物學意義。
注:Subba Reddy Palli 教授是美國肯塔基大學(University of Kentucky)昆蟲學系主任,國際著名的昆蟲學家。