
組織免疫微環境既是機體清除腫瘤細胞的戰場,又可被教化成為支持腫瘤生長和轉移的土壤;調控/重建其抗腫瘤功能是有效的腫瘤防治新策略。髓系免疫細胞(包括粒細胞、單核/巨噬細胞、髓源抑制性細胞和樹突狀細胞等)是免疫微環境的重要組分,可顯著影響腫瘤的發生發展以及對治療的應答。然而,過往對腫瘤相關髓系細胞的研究主要關注單個細胞亞群。受限于髓系細胞亞群的高度異質性和復雜的相互作用,我們目前仍難以對組織中的髓系免疫反應進行全局評估,也缺乏相應的臨床判斷指標。
我校生命科學學院鄭利民教授團隊利用來自國內三個中心的一千余例肝癌組織樣本,通過組織免疫化學原位染色獲得18個髓系反應特征,并通過Lasso Cox正則回歸模型將這18個髓系反應特征擬合患者臨床數據,最終構建出一個技術上簡單(只需2個髓系標記)而臨床上可靠的“髓系反應評分”(myeloid response score,MRS)。課題組利用多種腫瘤免疫學研究技術并結合癌癥基因圖譜(TCGA)數據庫的數據分析,揭示:MRS反映了肝癌組織浸潤的抗腫瘤與抑腫瘤髓系細胞亞群的變化,指示組織微環境中的髓系反應平衡狀態,并與CD8+ T細胞的免疫耐受密切相關。在多中心、大樣本的檢驗中,這一簡單而穩定的MRS評分與患者術后復發和死亡風險顯著相關,是肝癌的獨立預后因子,并優于多種臨床現用的判斷指標。因此,MRS的提出將有助于更全面地評估腫瘤免疫微環境特性,并為預測肝癌患者的臨床預后和藥物響應提供基礎。
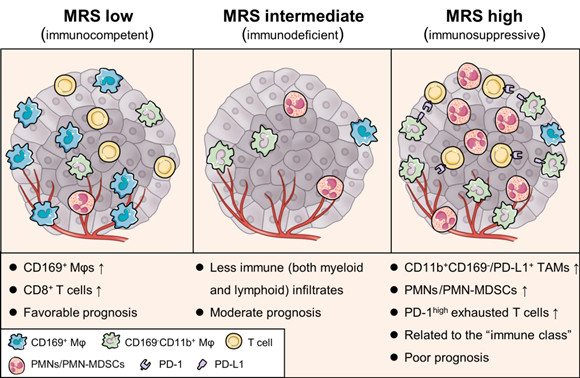
髓系反應評分MRS有助于更全面地評估腫瘤免疫微環境特性
研究結果以“Myeloid signature reveals immune contexture and predicts the prognosis of hepatocellular carcinoma”為題,近日,線上發表于權威醫學雜志Journal of Clinical Investigation (H-index:471)。生命科學學院特聘副研究員吳翀和博士生林潔為該論文的共同第一作者,鄭利民教授為獨立通訊作者。該研究與2018年該課題組以吳翀博士為第一作者發表在同一雜志的前期工作(J Clin Invest, 2018. 128(8): 3425-38),共同為揭示肝癌中的促腫瘤髓系反應的起源和平衡提供了重要的新認識。該研究受到國家科技重大專項、國家自然科學基金和中央高校基本科研業務費等基金資助。