
近年來,在了解鉑類藥物的細胞內行為方面取得了很大進展,但目前常用的活細胞內鉑類藥物的可視化方法均采用共聚焦顯微鏡,難以實現對超微結構的動態跟蹤。在不同的細胞成像顯微鏡中,超分辨率顯微鏡提供了一種突破光學衍射極限的超分辨成像技術,實現了對細胞器動態變化的超分辨率監測和藥物篩選。利用超分辨率成像實時跟蹤鉑類藥物,闡明其在活細胞中的行為和分布等作用機制,對鉑類藥物開發具有重要意義。然而,設計光物理性質優異、可用于超分辨成像的小分子化合物仍然是一個挑戰。
近日,我校化學學院毛宗萬教授團隊、辛辛那提大學刁佳杰教授團隊和香港大學任詠華教授團隊合作報道了一個可用于超分辨成像的雙核鉑配合物(Pt2L)。該配合物具有超大的Stokes位移和優異的光物理性能,極大地降低了超分辨成像的背景。同時該配合物具有高的耐光漂白性能,可實現活細胞內的長時間追蹤。
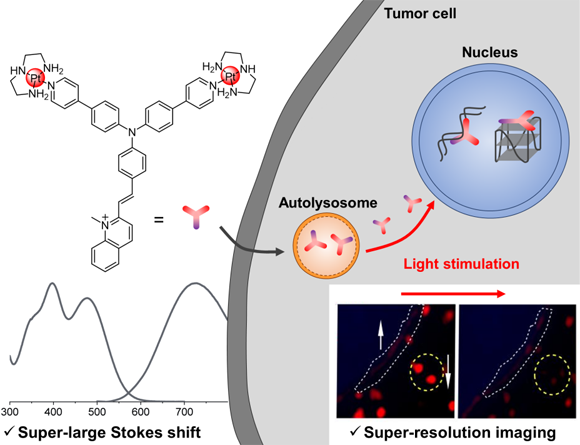
該配合物主要定位于自噬溶酶體,可追溯自噬變化。另外,該配合物在光刺激下可從溶酶體逃逸到細胞核,并與細胞核的雙鏈DNA和G-四鏈體DNA作用。利用超分辨成像,研究團隊第一次觀察到鉑配合物從自噬溶酶體到細胞核的逃逸路徑。利用其光激活逃逸特性,可以通過光照選擇地調控鉑配合物Pt2L從自噬溶酶體到細胞核,為提高核酸靶向鉑類化合物的光動力療效提供了新的途徑。
這一研究工作不僅為鉑配合物在活細胞內超分辨成像、探測自噬變化、且為提高鉑類化合物的靶向性提供了光刺激從自噬溶酶體逃逸到細胞核的新途徑。相關研究成果近期發表在化學頂級期刊《德國應用化學》,題目為“Multiple‐Color Platinum Complex with Super‐Large Stokes Shift for Super‐Resolution Imaging of Autolysosome Escape”, Angew. Chem. Int. Ed. 2020, 59, 19229-19236.
我校在讀博士研究生劉柳宜為論文的第一作者,辛辛那提大學博士研究生方紅寶,山東第一醫科大學副研究員陳啟鑫和香港大學博士后陳皓揚為論文的共同第一作者,我校毛宗萬教授、辛辛那提大學刁佳杰教授和香港大學任詠華教授為通訊作者。
上述研究工作得到了國家自然科學基金、教育部創新團隊和中央高校基礎研究經費等項目的資助。