
流感病毒種類多,宿主范圍廣,廣泛分布在野鳥、水禽、陸禽等多種自然宿主中,近年來,越來越多禽流感病毒跨宿主傳播感染人類,嚴重危害人類健康,同時給全球公共衛生安全帶來重大挑戰,目前,可以感染人類的禽流感病毒主要包括H5N1、H5N6、H7N9以及H9N2等。這些病毒不斷跨種傳播的現象提醒我們,再次發生流感大流行的威脅始終存在,世界衛生組織也一直將流感大流行作為人類面臨的十大公共衛生威脅之一(https://www.who.int/news-room/feature-stories/ten-threats-to-global-health-in-2019)。
2013年春,舒躍龍教授團隊在國際上首次報道一種新型重配低致病性H7N9禽流感病毒(Low pathogenic avian influenza A(H7N9) virus,LPAI H7N9)可導致人的感染和死亡(NEJM 2013)。H7N9禽流感病毒在人群中共造成了五波流行,導致我國內地1537人感染,其中612例死亡,病死率約39.8%。流行病學研究證明活禽市場和家禽暴露是感染H7N9禽流感病毒的主要風險因素,但H7N9禽流感病例中,職業暴露人群(與家禽養殖、運輸以及銷售等有關的從業人員)只占總確診人數的7%。那么,相同暴露條件下,為何只有很少的人會感染H7N9禽流感病毒,而大部分人則不被感染,仍是未解之謎。
為了攻克這個難題,舒躍龍教授團隊推測宿主遺傳因素可能發揮了重要作用。為了證明這個假設,團隊采用病例對照研究方法,共納入217例H7N9禽流感確診病例(real time RT-PCR檢測陽性)和116例與確診病例具有流行病學關聯的職業暴露人群對照(real time RT-PCR檢測陰性),收集樣本并進行人全基因組測序。通過全基因組關聯分析和Gene-base關聯分析,首次發現人MX1基因稀有變異可能增加人感染H7N9禽流感病毒風險。
抗粘液病毒基因(Myxovirus resistant, Mx)是最早發現的干擾素誘導的抗病毒基因之一,人MX1基因可編碼人抗黏液病毒蛋白A(Human myxovirus resistance protein A, MxA),MxA蛋白屬于動態蛋白超家族的一類大分子GTPase,對多種RNA病毒和DNA病毒具有抗病毒作用,包括甲型流感病毒和乙型肝炎病毒等。進一步的研究結果表明,H7N9禽流感病例中共發現了17個MX1稀有變異,包括15個錯義突變、1個無義突變和1個剪切位點突變。體外實驗驗證表明,其中14個變異會影響蛋白功能。流感聚合酶活性實驗及病毒感染實驗表明,這14個攜帶突變的MxA蛋白不僅失去對H7N9禽流感病毒的抑制作用,也失去對H7N7和H5N1禽流感病毒的抑制作用,同時也失去對pdmH1N1流感的抑制作用。經過一代測序驗證,H7N9病例攜帶的MX1 稀有突變全部為雜合突變,那么野生型MxA是否在體內繼續發揮抗病毒作用呢?研究團隊進一步開展了MxA突變體對野生型MxA的顯性負效應研究,結果表明有12個失去抗病毒活性的MxA突變體對野生型MxA具有顯性負效應,說明MX1雜合子不受保護。這項研究首次發現與人感染H7N9禽流感病毒風險增加相關的MX1基因變異,進一步通過體外實驗驗證,MX1基因稀有變異可以增加人感染禽流感病毒風險。研究結果首次解釋了相同暴露條件下,為何只有一小部分人會感染H7N9禽流感病毒這一流行病學現象,同時這些變異均為稀有變異,在人群中的變異頻率小于0.5%,間接提示H7N9禽流感病毒目前導致流感大流行的風險較低;研究結果也為將來可能的高危人群監測提供了科學依據,進一步推動傳染病精準防控。
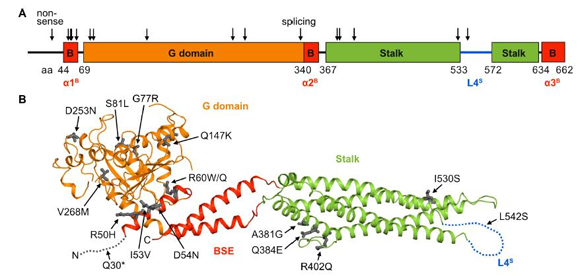
H7N9禽流感病例中發現的MX1稀有變異示意圖
上述研究工作以“Rare variant MX1 alleles increase human susceptibility to zoonotic H7N9 influenza virus ”為題,于2021年8月20日在線發表在Science期刊。我校公共衛生學院(深圳)陳永坤博士、德國弗萊堡大學博士后Laura Graf、我校公共衛生學院(深圳)博士研究生廖啟軍和中國疾病預防控制中心病毒病預防控制所陳濤副研究員為論文共同第一作者,我校公共衛生學院(深圳)舒躍龍教授、德國弗萊堡大學Martin Schwemmle教授和中國疾病預防控制中心病毒病預防控制所王大燕研究員為共同通訊作者。本研究得到國家重點研發計劃和深圳市科技計劃項目的支持。